

Les caractéristiques des solvants organiques.
Exemples des solvants de dégraissages en industrie.
A. Séchage et volatilité des solvants
organiques :
B. Pouvoir solvant,
et caractéristiques techniques :
C. Point
éclair (Pe) et inflammabilité des solvants
D. Valeurs
limites d’exposition et risques produits
A. Articles
et études théoriques dans la littérature.
B. Etudes et tests réalisés en milieux
industriels
Regroupement et analyse des résultats : CONCLUSION
Figure 1 : Caractéristiques générales des solvants organiques.
Les indices d’évaporations relatifs à l’éther éthylique (Ie, norme DIN 53170) et à l’acétate de butyle (Iab, normes DIN 53170 et ASTM D 3539) permettent de classer les solvants en trois grandes classes :
1. Séchage lent, plus de 30 minutes, Ie>15 ou Iab<0.2
2. Séchage moyen, de 1 à 30 minutes, 3<Ie<15 ou 0.2<Iab<1
3. Séchage rapide, moins dune minute, Ie<3 ou Iab>1.
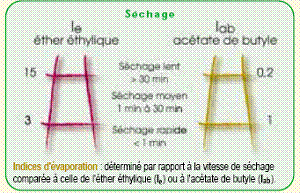
Figure 2 : Mesure de la vitesse de séchage des solvants
La pression de vapeur des produits est reliée à la volatilité et au temps de séchage des produits. Plus la tension de vapeur est élevée et plus le produit est volatil.
Différentes méthodes normalisées existent :
· Indice Kauri butanol (norme ASTM D 1133) : méthode représentative uniquement pour les salissures de type gommes, caoutchouc, résines… Plus l’indice KB est important meilleur est le pouvoir solvant du produit
· Point d'aniline (norme ASTM D 611) : méthode particulièrement adaptée au choix des solvants hydrocarbonés, convenant à la majorité des cas du travail des métaux.
Nous avons utilisé pour nos calculs de pouvoir solvants les paramètre de solubilité de Hildebrand et Hansen. Cette méthode théorique, nous a permis de définir les meilleurs mélanges de solvants à tester au laboratoire.
La quantification de la faculté qu'ont des produits à s'enflammer est donnée par leur point d'éclair. Le point éclair est la température minimale pour laquelle un liquide émet des vapeurs en quantités telles, qu’il en résulte un mélange air/vapeur inflammable. Plus le point éclair est élevée, moins le produits est inflammable :
La substance ou la préparation est affectée d'une étiquette définie en fonction de critères de classification suivants:
|
Point d'éclair |
< 0° C |
0°C< Pe <21°C |
21°C< Pe <55°C |
> 55°C |
|
température d'ébullition |
< à 35° C |
|
|
|
|
Classe |
Symbole F+ |
Symbole F |
|
Pas de point éclair |
|
phrase de risque |
R12 (Extrêmement inflammable) |
R 11 (Facilement inflammable) |
R 10 (Inflammable) |
Peut devenir inflammable en cours d'utilisation |
Tableau 1 : Point éclairs et inflammabilité.
Certaines remarques sont à faire à propos des solvants halogénés, en effet, le protocole habituel de mesure d'un point d'éclair est mal adapté (ainsi, selon la norme EN 456 : «…, l'interprétation des résultats obtenus sur les mélanges de solvants contenant des hydrocarbures halogénés doit être faite avec prudence car ces mélanges peuvent donner des résultats aberrants »).
Pour évaluer les dangers des solvants, il faut prendre en compte la valeur limite d'exposition professionnelle de chacun de leurs constituants. Cette valeur limite correspond à une concentration dans l'air que peut respirer une personne pendant un temps donné sans risque d'altération pour la santé même si des modifications physiologiques sont parfois tolérées :
VLE : valeur limite d'exposition à court terme. C'est la valeur maximale mesurée sur 15 minutes à laquelle peut être exposé un opérateur sans risque d'effets toxiques immédiats.
VME : valeur de moyenne d'exposition. C'est la valeur moyenne maximale admissible pondérée pour 8 h/j et 40 h/semaine de travail.
L’évolution de la réglementation internationale (Protocole de Montréal et Directive Européenne « substances dangereuses ») et la volonté de prévention des risques professionnels, conduisent les industriels à chercher de nouveaux produits de substitutions à divers solvants de dégraissages halogénés, largement utilisés jusqu’à présent en industrie.
La substitution du trichloréthylène (classement cancérogène), du 1,1,1-trichloroéthane (T 111), du tétrachloroéthylène (perchloroéthylène), du 1,1,2-trichloro-1,2,2-trifluoroéthane (CFC 113), du dichlorométhane (chlorure de méthylène) et du HCFC 141b (monochlorotrifluoroéthane) sont notamment des mesures prioritaire depuis 2001.
Les solvants de substitutions envisagés devront être moins toxique pour l’Homme, tout en gardant des qualités aussi bonnes que les solvants halogénés en cours de remplacement :
· Compatibilité avec l’environnement (VLE, VME),
· Utilisables à chaud et froid…
D’après de nombreuses études et recherche industrielles et en laboratoires, les solvants de substitution des solvants chlorés dans l’industrie sont :
Ces solvants sont les plus appropriés pour substituer les solvants chlorés.
Dans différents pays, les industriels et laboratoires de recherches ont publiés de nombreuses études et articles, nous présentons les études les plus importantes réalisées dans les dernières années.
Nous nous sommes appuyés sur 5 articles particulièrement intéressants :
Une des premières études en
milieu industriel a eu pour but de tester 5 solvants de remplacement du
trichloréthylène : 1-bromopropane, HCFC-141b, 1-methoxy-2-propanol...
(A Study on the
Substitution of Trichloroethylene as a Spot Remover in the Textile Industry, T. Mirzaa, M. Gérina, D. Bégina, D. Droletb. AIHAJ, 61, 2000. Université de Montréal, Groupe de
recherche en toxicologie humaine (TOXHUM), Département de santé
environnementale et santé au travail).
Une autre étude, Substitution des solvants – Études de cas d’implantation, D. Bégin, M. Gérin. Département de santé environnementale et santé au travail. Faculté de médecine, Université de Montréal (février 2001) conclut qu’il n’y pas de substituants envisageables au trichloréthylène.
Le nombre d’études sur ce sujet et très vaste, mais généralement ces études mènent à la conclusion qu’aucun solvant de substitution aux solvants halogénés ne conviennent.
Les solvants les plus fréquemment proposés sont présentés dans la figure
suivante
-->Consultez le document Risques spécifiques * Dégraissage des métaux sur le site de la CRAM des Pays de la Loire pour plus de détails


Figure 3 : Tables de comparaison des solvants alternatifs
Les solvants de substitutions envisageables sont donc nombreux, seuls les solvants qui ont été le plus couramment utilisés, ou proposés sont reportés dans le tableau ci-dessous.
|
|
méthoxy propanol |
NMP |
1-bromo propane |
d-Limonene |
trichloro et Hydrofluoro |
|
Indice Kb |
élevé |
> 300 |
élevé |
67 |
90 à
150 |
|
Risques |
R10 inflammable |
Xi irritant |
Xn nocif |
aucun |
XN nocif |
|
VME |
360 |
15 |
20 |
aucune |
>100 |
|
volatilité |
volatil |
peu volatil |
peu volatil |
peu volatil |
très
volatils |
|
Point éclair |
34°C |
91°C |
aucun |
48°C |
aucun |
|
Séchage (ether=1) |
25 long |
360 long |
long |
long |
rapide |
|
incompatibilté |
Zn, Cd |
Zn |
- |
Zn, Al |
- |
|
densité |
0,92 |
1,028 |
1,354 |
0,84 |
|
Tableau 2 : Récapitulatifs des solvants choisis
Les conclusions des rapports
industriels et théoriques sont unanimes et décommandent le 1-bromopropane. De plus le bromopropane est sujet d’une
nouvelle réglementation applicable à l’ensemble des pays européens en 2006
(article INRS : Le 1-bromopropane sur la sellette), sa classification
évoluant vers la catégorie 2 des toxiques pour la reproduction, va conduire le
bromopropane à être soumis au décret CMR (décret 2001-37 du 1er février
2001. Le trichloréthylène, étiqueté cancérogène de catégorie 2, est soumis à ce
décret.
·
« Considérant la toxicité potentielle du 1-BP sur le système
nerveux et sur la reproduction chez
l’humain,
sa tension de vapeur élevée qui favorise sa migration dans l’air des locaux de
travail, l’ambiguïté sur son point d’éclair et secondairement l’incertitude sur
son PDO, les auteurs ne recommandent pas cette substance comme remplaçant des
solvants chlorés traditionnels »
·
« Un
test sur 11 personnes en 2000 en milieu industriel a conclu dès le premier jour
d’étude suite aux
irritations des yoeux et de la gorge des
travailleurs que le bromopropane était inenvisageable »
·
Autres
références :MAHIEU J.C.
; BOUST C."Dégraissage des métaux, choix des techniques et des
produits".
Fiche pratique de sécurité. ED 48. INRS, 2001, 4 p. et BEGIN D. ; GERIN M. "Le 1-bromopropane
et la substitution des solvants". Rapport B-062. IRSST, 2002, 75 p.
Le 1-méthoxy-2-propanol est « facilement biodégradable » d'après
les résultats de l’essais n°301E de l'Organisation de coopération et de
développement économiques (OCDE).
Le 1-méthoxy-2-propanol, isomère alpha, CAS number 107-98-2, d’après sa fiche solvant ED 4222, les ethers de glycols, INRS, 2004, ne présente que le risque R10, Inflammable.
Ce solvant est utilisé dans de nombreux solvants de dégraissages.
Ce solvant est un des solvants potentiellement le plus approprié pour substituer les solvants chlorés. Il est déjà utilisé dans de nombreuses formulations, une simple recherche Internet conduit à trouver plusieurs centaines de produits de dégraissages contenant le limonène.
![]()