Réactions de substitution nucléophile et d’élimination
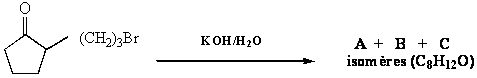
I- Compléter
les réactions suivantes, préciser la nature du processus de la réaction
d’élimination.
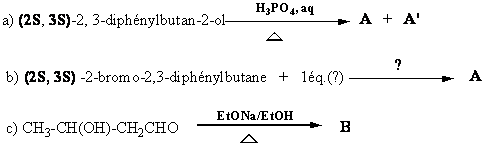
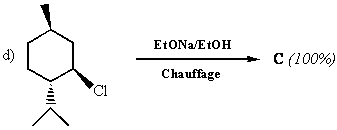

-Comment peut-on distinguer C
de D par RMN 1H ?
![]()
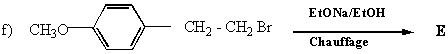
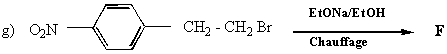
![]()
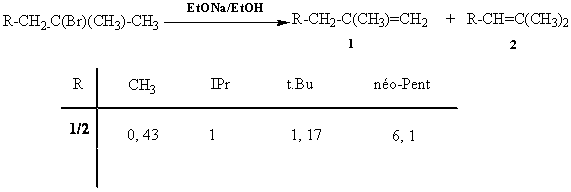
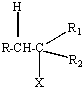
II-Expliquer la
régiosélectivité observée en fonction de la nature de R pour la réaction:
III-
a) Proposer un mécanisme pour la
réaction suivante :

b) Le remplacement de OH peut être réaliser comme ci-dessous
:
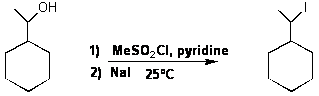
Décrire le mécanisme de chacune des
étapes. Le remplacement de MeSO2Cl
par CF3SO2Cl
peut-il accélérer la deuxième étape? Pourquoi?
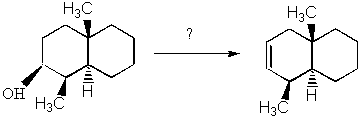
IV-Quel est le mécanisme de la réaction ci-dessous ?

V - Quel produit
majoritaire obtient-on dans les réactions suivantes ?
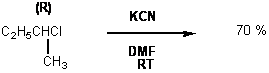
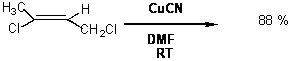
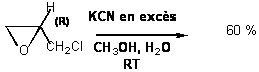
Représenter la configuration absolue des carbones
asymétriques et préciser le mécanisme de cette dernière réaction sachant
qu’elle met en jeu la formation d’un
autre époxyde.
VI-
Soient les réactions suivantes :
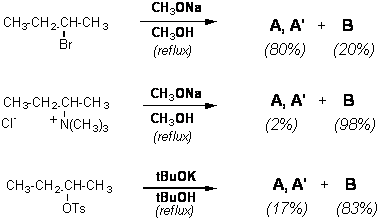
A, A’ et B sont isomères
Justifiez l’obtention de chacun de ces produits et de leurs
proportions.
VII- On soumet le (2R)-bromobutane à l’action de :
a) [(CH3)2
CH]2 Nli
dans le tétrahydrofurane.
b) CH3ONa dans
le méthanol.
c) CH3SNa dans
l’acétone.
d) CH3OH.
Indiquer les produits obtenus et préciser le mécanisme.
VIII- Dans les transformations suivantes,
le produit C est optiquement actif lorsqu’on utilise le stéréo isomère
actif A, mais racémique lorsqu’on emploie le stéréo isomère A’.
La transformation B’® C’ est
beaucoup plus rapide que la transformation B ® C parce que cette transformation correspond à une
substitution avec participation d’un groupe voisin (ici le groupe acétate) et
qu’une des caractéristiques d’une telle transformation est une augmentation
très importante de la vitesse de cette transformation.

1) Donner les formules développées de B, C et B’.
![]() 2) Proposer un mécanisme pour la transformation
suivante : B D (optiquement
actif).
2) Proposer un mécanisme pour la transformation
suivante : B D (optiquement
actif).
3) Représenter le racémique D’.
4) Proposer une formule
développée pour l’intermédiaire réactionnel cyclique à 5 centres [I]
permettant l’obtention de D’ (racémique).
5) Donner la
configuration des carbones asymétriques de A et A’.
6) Quelle relation de
stéréochimie existe-t-il entre A et A’ ? Sont-ils isomères
de configuration ou de conformation ?
7) Représenter le
conformère de D, obtenu lors de la première transformation, c’est à dire
sous forme optiquement active et sous sa conformation la plus stable.
Données :
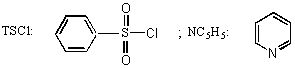
IX- Préciser le mécanisme des réactions
suivantes :
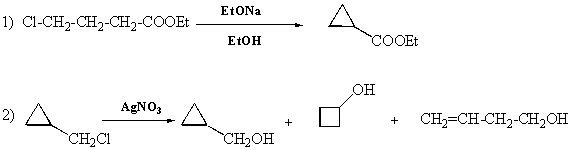
3)
X- Soit la séquence
réactionnelle ci-dessous :

a. Représenter A dans sa configuration R.
b. Ecrire l’équation de la
réaction permettant de transformer A
en B. Cette transformation est-elle
totale ? Justifier.
c. De quelle réaction s’agit-il
dans la transformation de D en C1 ? Préciser la loi de
vitesse, le mécanisme et la stéréochimie dynamique de cette transformation.
d. De quelles réactions s’agit-il
dans les transformations A en D, A
en C2 et B en C3 ?
e. Donner la formule développée
de C2.
f. C2 est-il chiral ? Justifier.
g. Quelle relation de stéréochimie
existe-il entre C1, C2
et C3, isomères
de position, de fonction…, identiques ou énantiomères ? Justifier.
XI- L’halogénure ci-dessous est traité
par l’éthylate de sodium.
1) Donner les 2 produits
obtenus pour R=R1=H et R2=CH3.
2) Donner l’expression de
la vitesse de ces 2 réactions compétitives.
3) Pour R1=R2=CH3,
lequel des 2 produits sera majoritaire ? Justifiez votre choix
4) ![]() Même question si R= COCH3.
Même question si R= COCH3.
5) Donner le produit
majoritaire de cette réaction si l’halogénure est traité par :
a) l’amidure
de sodium
b) le cyanure de sodium
6) Donner le produit majoritaire si le solvant utilisé pour cette
réaction est le DMF (Diméthyle formamide)
XII- Compléter :
XIII-
|
Matériel |
Produit
|
|
4 tubes à essai +
support |
Bromure de n-butyle |
|
|
Bromure de tert-butyle |
|
|
Solution d’iodure de sodium à 15% |
|
|
Solution de nitrate d’argent dans
l’éthanol absolu à 2% |
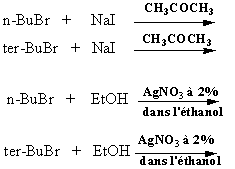
Mode opératoire.
1) Placer 10mL de solution
d’iodure de sodium dans un des tubes. Y ajouter 10 gouttes de bromure de n-butyle. Répéter l’opération avec le bromure de tertio-butyle. Dans le premier tube, le bromure de
sodium précipite en 3 minutes, alors qu’il lui faut une heure pour apparaître
dans le deuxième.
2) Reprendre le mode
opératoire donné en 1) en utilisant la solution de nitrate d’argent dans
l’éthanol à la place de la solution d’iodure de sodium. Dans le tube
contenant le dérivé bromé primaire, le bromure d’argent se forme en 15
secondes. Il se forme instantanément dans le tube contenant le dérivé bromé
tertiaire.
Discussion.
1) Donner les équations de
ces différentes réactions.
2) Quel est pour la
première expérience le nucléophile ? Quel est pour la première expérience
le nucléofuge?
3) Donner le mécanisme de
ces 2 expériences.
4) Donner les facteurs
favorisant l’expérience 1).
5) Donner les facteurs
favorisant l’expérience 2).
6) Comment justifiez vous
la plus grande réactivité du bromure de tertio-butyle dans
l’expérience 2)?