Les applications récentes :
Synthèse de pyrroles :
Depuis une quinzaine d’année, les travaux effectués ont permis de mettre au point la synthèse de pyrroles en passant au préalable par une condensation aldolique croisée de type Mukaiyama.
Les chimistes ont reportés en 1988
la synthèse de N-acyl-trialkylpyrroles à partir
d’éthers silylés d’énol et
du diméthylacétal (schéma). Cette synthèse a pour
particularité de créer la liaison C-C en premier pour fournir le b-céto-acétal,
puis la liaison C-N intervient en second lieu lors de la cyclisation menant au pyrroles.
Bilan de la réaction :

Une voie de synthèse de pyrroles
tricycliques a également été réalisé en passant par la
réaction de Mukaiyama.
Par ailleurs en 1990, des
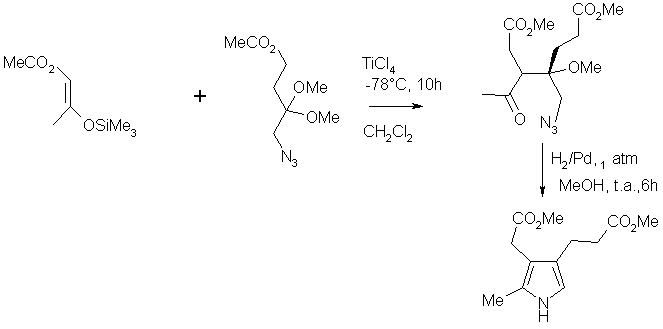
chercheurs ont fait intervenir un a-azido-acétal comme électrophile.
Le produit de couplage avec l’éther d’énol silylé donne un produit intermédiaire le b-céto-acétal,
qui une fois hydrogénée, libère l’amine et cyclise comme précédemment.
Bilan de la réaction :
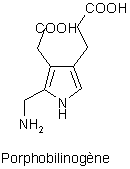
De telle réactions permettent d’imaginer de nouvelle voie de synthèse pour des composés comme le Porphobilinogène (PBG), qui est un intermédiaire destiné à la biosynthèse des tétrapyrroles. Ces pigments tétrapyrroliques jouent un rôle important dans les processus fondamentaux de la vie. On peut citer l’hème permettant le transport d’oxygène et d’électrons, où encore la chlorophylle, qui collecte les photons de la lumière et les transforme en énergie.
D’autres
voie de synthèse de ce composé ont été trouvé en
faisant intervenir un cyanure d’acyle comme électrophile, afin de compenser la
faible nucléophilie de l’éther silylé d’énol.